Inom diabetesforskningen screenas personer som är i riskzonen för att utveckla typ 1-diabetes.
Dagens metod innebär att det tas flera blodprov vid varje besök.
Ett internationellt forskarlag har nu upptäckt att det går att följa upp risken för sjukdom med ett enkelt stick i fingret.
Både barn och vuxna kan få typ 1-diabetes, som kräver behandling med insulin hela livet. Symtomen kan utvecklas under lång tid och kan ibland vara svåra att lägga märke till. De metoder som har etablerats inom forskningen för att upptäcka förstadier till typ 1-diabetes är resurskrävande. Ett internationellt forskarlag har nu utvecklat ett test som gör att det går att förutsäga sjukdomen på ett enklare sätt.
– I stället för att lämna en större mängd blod genom en ven i armen varje gång räcker det med ett stick i fingret per besök. Det kommer att innebära mindre obehag för personer som screenas för typ 1-diabetes säger Åke Lernmark, senior professor i experimentell diabetes vid Lunds universitet och korresponderande författare för studien.
Följer utvecklingen
Studien publiceras nu i den vetenskapliga tidskriften Diabetologia och bygger på data från deltagare upp till 45 år i studierna DPT-1, Trialnet, Teddy och Fr1da. Samtliga deltagare hade nått det första eller andra stadiet av typ 1-diabetes. En diagnos brukar ställas först på tredje stadiet.
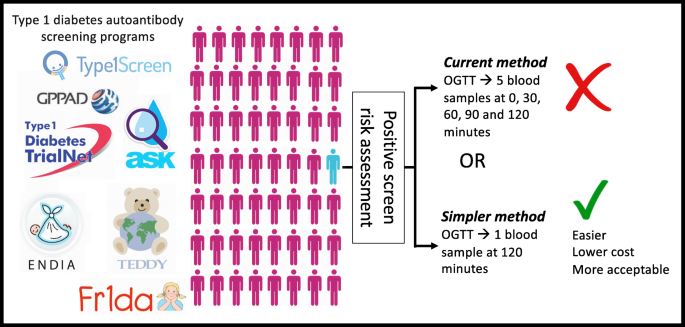
För att avgöra var på utvecklingskurvan forskningsdeltagare befinner sig görs glukostoleranstester (OGTT) ett par gånger om året. Vid ett sådant test kommer personen fastande till mottagningen och får lämna ett blodprov som anger utgångsvärdet. Sedan får personen dricka en lösning med glukos. Därefter tas nya blodprov efter 30, 60, 90 och 120 minuter för att se hur blodglukosvärdet utvecklas.
Störst precision
Forskarna har jämfört ett stort antal glukostoleranstester som hade gjorts över flera års tid på sammanlagt omkring 3500 individer. Analyserna visade att det blodprov som togs två timmar efter glukoslösningen kunde förutse risken för att få diagnosen typ 1-diabetes med störst precision.
– Vi har länge trott att vi behöver ta blodprov med täta intervaller för att göra en så bra analys som möjligt, men det var tvåtimmarsvärdet som bäst talade om för oss att en person var på väg att få sin diagnos. Jag och mina forskarkollegor blev väldigt förvånade över det här, säger John Wentworth, huvudförfattare verksam vid Royal Melbourne Hospital och Walter and Eliza Hall institute i Australien.
Screening för typ 1-diabetes ökar i länder som USA. I Sverige är det framför allt inom olika forskningsprojekt som metoden används för att förutse sjukdomen. Ett sådant exempel är den svenska delen av den internationella Teddy-studien, som bekostas av den amerikanska hälsovårdsmyndigheten (NIH). Sverige har inget screeningprogram för personer som är i riskzonen för att få typ 1-diabetes.
– Den svenska sjukvården ”screenar inte för sjukdomar som inte går att förebygga, förhindra eller bota”.
Du kan visserligen inte bota diabetes med insulin, men en tidig upptäckt av sjukdomen minskar risken för komplikationer, Åke Lernmark, som är verksam vid Lunds universitets diabetescentrum (LUDC).
Viktig kunskap
Typ 1-diabetes som inte är tillräckligt behandlad kan leda till höga blodglukosvärden. Det kan i sin tur leda till ketoacidos, som kan bli livshotande om det inte behandlas. I Teddy-studien screenas barn som är i riskzonen och de som är på väg att utveckla typ 1-diabetes upptäcks i ett tidigt skede.
– Många av föräldrarna är så tacksamma för de är beredda när sjukdomen kommer. Vi har föräldrar som säger ”Tack vare Teddy har vi sluppit sitta på akuten med ett barn som har blivit riktigt sjukt i ketoacidos”, säger Åke Lernmark, som är vetenskapligt ansvarig för Teddy-studien i Sverige.
Den förenklade screeningmetoden kommer att vara till hjälp för forskarna i arbetet med att lära sig mer om hur sjukdomen utvecklas. Kunskapen är viktig för det strategiska forskningsområdet Exodiab vid Lunds universitet. Exodiab har som mål att förebygga och bota diabetessjukdomar.
– Nu har vi hittat en metod som gör det enklare att screena, vilket kommer att spara mycket tid och resurser för oss. Vi hoppas att det kan skynda på vårt arbete med att hitta ett läkemedel som kan stoppa sjukdomen från att bryta ut, säger Åke Lernmark, som är en del av forskningsmiljön Exodiab.
Av: Petra Olsson
Studien i Diabetologia
Artikeln ”Simplifying prediction of disease progression in pre-symptomatic type 1 diabetes using a single blood sample” är publicerad i den vetenskapliga tidskriften Diabetologia, augusti 2021, DOI: https://doi.org/10.1007/s00125-021-05523-2
Korta fakta om studien
Ämne: Typ 1-diabetes (så kallad autoimmun diabetes)
Forskningsområde: Klinisk forskning
Typ av publicering: Peer review-granskad publikation
Studiedesign: Kvantitativ studie, forskarinitierad studie, statistiska samband
Experimentell undersökning: In vivo
Observationsstudie: Prospektiv, longitudinell, friska frivilliga
Antal grupper i studien: Fyra grupper. 601 individer från DPT-1, 2684 personer från Trialnet (TN-01), 209 personer från Teddy och 80 individer från Fr1da.
Antal forskningspersoner i studien: 3574
Press release
Läs hela studien i Diabetologia pdf utan kostnad, abstract och artikel
https://doi.org/10.1007/s00125-021-05523-2
Simplifying prediction of disease progression in pre-symptomatic type 1 diabetes using a single blood sample. Diabetologia
- Naiara G. Bediaga,
- Connie S. N. Li-Wai-Suen,
- Michael J. Haller,
- Stephen E. Gitelman,
- Carmella Evans-Molina,
- Peter A. Gottlieb,
- Markus Hippich,
- Anette-Gabriele Ziegler,
- Ake Lernmark,
- Linda A. DiMeglio,
- Diane K. Wherrett,
- Peter G. Colman,
- Leonard C. Harrison &
- John M. Wentworth
Diabetologia 2021
Abstract
Aims/hypothesis
Accurate prediction of disease progression in individuals with pre-symptomatic type 1 diabetes has potential to prevent ketoacidosis and accelerate development of disease-modifying therapies. Current tools for predicting risk require multiple blood samples taken during an OGTT. Our aim was to develop and validate a simpler tool based on a single blood draw.
Methods
Models to predict disease progression using a single OGTT time point (0, 30, 60, 90 or 120 min) were developed using TrialNet data collected from relatives with type 1 diabetes and validated in independent populations at high genetic risk of type 1 diabetes (TrialNet, Diabetes Prevention Trial–Type 1, The Environmental Determinants of Diabetes in the Young [1]) and in a general population of Bavarian children who participated in Fr1da.
Results
Cox proportional hazards models combining plasma glucose, C-peptide, sex, age, BMI, HbA1cand insulinoma antigen-2 autoantibody status predicted disease progression in all populations. In TrialNet, the AUC for receiver operating characteristic curves for models named M60, M90 and M120, based on sampling at 60, 90 and 120 min, was 0.760, 0.761 and 0.745, respectively. These were not significantly different from the AUC of 0.760 for the gold standard Diabetes Prevention Trial Risk Score, which requires five OGTT blood samples. In TEDDY, where only 120 min blood sampling had been performed, the M120 AUC was 0.865. In Fr1da, the M120 AUC of 0.742 was significantly greater than the M60 AUC of 0.615.
Conclusions/interpretation
Prediction models based on a single OGTT blood draw accurately predict disease progression from stage 1 or 2 to stage 3 type 1 diabetes. The operational simplicity of M120, its validity across different at-risk populations and the requirement for 120 min sampling to stage type 1 diabetes suggest M120 could be readily applied to decrease the cost and complexity of risk stratification.
Graphical abstract

Utdrag ur artikeln
Discussion
We describe models to predict progression to insulin-dependent type 1 diabetes that are simpler than the previously validated DPTRS, DPTRS60 and Index60 risk scores and yet have comparable performance in the contemporary TrialNet and Fr1da populations. The models incorporated sex, age, BMI, HbA1c and IA-2A status in combinations with glucose and C-peptide measures that are the basis of the DPTRS, DPTRS60 and Index60. In contrast to DPTRS, DPTRS60 and Index60, the new models focus on a single-time-point blood sample during the OGTT, decreasing the cost associated with analyte measurement. In addition, they do not require venous cannulation, which adds complexity and discomfort, particularly in young children. M60 and M90 were the most accurate single-time-point models in TrialNet. However, M120, based on a 120 min blood sample that is routinely used to stage type 1 diabetes, performed well in all populations other than DPT-1 and might therefore be best suited to current screening programmes of at-risk relatives [6] and, potentially, the general population [7, 8].
The universal use of sex, HbA1c and IA-2A status by all single-time-point models suggests that their incorporation into DPTRS and DPTRS60 might improve the performance of these models, and that the performance of Index60 could be augmented by these measures together with age and BMI. Age, HbA1c and IA-2A status are recognised risk factors for disease progression [7, 14, 28,29,30], and sex and BMI have been associated with progression to stage 3 diabetes in some [16, 30, 31], but not all [29], studies of autoantibody-positive people. Notably, although HLA-DR3 and -DR4 alleles have been described as predictors of progression from stage 1 to stage 3 disease in the TEDDY study [31], neither contributed to model performance.
Type 1 diabetes disease staging was introduced to educate the medical and lay communities about pre-symptomatic type 1 diabetes and the potential for its prevention using immune therapy [11]. Disease stages 1 and 2 also help classify the risk of progression to insulin dependence and have been used to define eligibility for prevention trials. Because disease staging requires a 120 min sample, M120 could be readily incorporated into current clinical workflows, thereby helping to improve clinical trial efficiency and, potentially, the identification of autoantibody-positive individuals at greatest risk of ketoacidosis, for whom education about symptoms of hyperglycaemia and close follow-up should be provided. It could also be used to identify individuals approaching insulin dependence who are currently best suited to receive immune therapy [4] as well as to identify high-risk single-antibody-positive individuals who would not currently meet entry criteria for TrialNet prevention trials. The key disadvantage of M120 compared with other single-time-point models is the time required to do the test, but perhaps this could be shortened if participants were provided with a kit that enabled them to record home fasting capillary blood glucose (for the purposes of type 1 diabetes staging), ingest glucose and then time their arrival to a collection centre for a single blood draw 120 min later.
In the TrialNet populations studied, the AUCs for the M60 and M90 models were greater than the AUCs of the other single-time-point models, and M60 performed better than M0, M30, M90 and M120 in DPT-1. These findings accord with a TrialNet study which demonstrated that a biphasic oral glucose response with a nadir at 60 or 90 min was associated with a low risk of disease progression [32], and the analysis of a combined DPT-1 and TrialNet dataset that formed the basis of the Index60 score, which identified 60 min measures of glucose and C-peptide as the strongest univariate predictors of stage 3 disease [17]. Overall, this suggests M60 could be used instead of DPTRS in TrialNet to simplify and decrease the cost of risk assessment, particularly if the 60 min glucose were used to diagnose diabetes mellitus, as suggested by other TrialNet studies [17, 18]. However, there has been a long-standing requirement for a 120 min glucose to diagnose diabetes mellitus [12], which is likely to endure. Furthermore, the very high M120 AUC of 0.865 in TEDDY and the superior performance of M120 relative to other models in Fr1da suggest that 120 min sampling might be optimal for disease staging and risk stratification outside of TrialNet.
When tested in DPT-1, the models developed in this study were less accurate than DPTRS, DPTRS60 and Index60. This discrepancy is at least in part because these three multiple-time-point models were developed using DPT-1 data [16,17,18], which differed from TrialNet with respect to age, autoantibody prevalence, HbA1c and C-peptide. These population differences might be explained by the requirement in DPT-1 for participants to screen positive for islet cell antibodies by indirect immunofluorescence, the use of different autoantibody and C-peptide assays in DPT-1 that at times were performed many years after sample collection and, potentially, by changes in the contribution of environment to disease risk since the start of DPT-1 [33].
Several caveats should be mentioned. First, because TrialNet, TEDDY and Fr1da enrolled mostly individuals of European descent and used similar laboratory methods to measure C-peptide and HbA1c, the performance of the models in different contexts remains unproven. In addition, the Fr1da population was relatively small and therefore under-powered to assess the validity of all of the models, and thus further testing will be needed to confirm the utility of M120 in a general population setting. Finally, the thresholds used to define high and low risk for survival analyses were based on median values, which may not be optimal for specific populations. This being said, the DPTRS threshold of 6.8 used to define risk of progression to stage 3 type 1 diabetes in the TrialNet validation population was between the previously recommended thresholds of 6.5 for low risk [34] and 7.0 to 7.5 for high risk [34, 35]. Therefore, the M120 score of 11.1 used to stratify the TrialNet validation population would appear to be a reasonable threshold to apply to future TrialNet participants with stage 1 or 2 type 1 diabetes.
In summary, unbiased selection methods were applied to TrialNet data to develop equations to predict disease progression in pre-symptomatic type 1 diabetes. The M120 model, based on a single blood draw at 120 min of the OGTT, was identified as a comparably accurate yet more practical tool than the DPTRS, DPTRS60 or Index60. Its validity in different at-risk populations and its operational simplicity make M120 broadly applicable to current screening programmes and, potentially, for more routine clinical use with the advent of disease-modifying therapies.
Nyhetsinfo
www red DiabetologNytt

